[식약처]1,2,4-트리하이드록시벤젠(1,2,4-trihydroxybenzene, 1,2,4-THB) 화장품(영구 염모제, 모…
첨부파일
-
- 첨부파일: 화장품.jpg (132.6K)498
짧은주소
본문
[식약처]1,2,4-트리하이드록시벤젠(1,2,4-trihydroxybenzene, 이하 1,2,4-THB) 화장품(영구 염모제, 모발염색 샴푸)에 사용금지
-‘화장품 안전기준 등에 관한 규정’ 개정(안) 의견수렴 절차 마쳐
□ 식품의약품안전처(처장 김강립)는 ‘화장품 안전기준 등에 관한 규정’의 행정예고가 마무리됨에 따라, 1,2,4-트리하이드록시벤젠(1,2,4-trihydroxybenzene, 이하 1,2,4-THB)을 화장품 사용금지 원료로 지정해 목록에 추가하는 개정절차를 추진합니다.
○ 식약처는 2012년부터 화장품에 사용할 수 없는 원료를 지정하고 그 밖의 원료는 사용할 수 있게 하는 ‘네거티브 리스트’ 방식으로 운영하고 있으며, 과학적으로 타당한 위해정보가 있는 경우 위해평가 등의 절차를 거쳐서 금지 목록에 추가하고 있습니다.
□ 1,2,4-THB는 ‘모발 염색 기능’을 갖는 물질로, 소비자안전성과학위원회(SCCS)에서 위해평가를 실시하고 그 결과에 따라 유럽집행위원회(EC)가 2020년 12월 유럽의 화장품 사용금지 목록에 추가했습니다.
□ 식약처는 유럽 SCCS의 평가보고서와 관련 문헌 등을 종합적으로 검토하여 위해평가를 실시(’19년 4월∼’20년 11월)하고, 이를 토대로 1,2,4-THB의 사용을 금지하는 내용으로 행정예고(’21년 12월 27일∼ ’22년 1월 17일) 했습니다.
○ 전문가 자문 회의에서는 행정예고 기간 중에 제출된 의견을 포함하여 1,2,4-THB에 대한 안전성을 종합적으로 검토하였고, 식약처는 잠재적인 유전독성 및 피부감작성 우려에 따라 사용금지 목록에 추가하는 것이 타당하다는 최종 결론을 도출했습니다.
※ 1,2,4-THB 위해평가(’19∼’20년), 행정예고(’21.12∼’22.1)
<식약처 위해평가 결과>
□ 식약처는 1,2,4-THB에 대한 안전성을 평가할 목적으로 유럽 SCCS의 평가보고서와 관련 문헌 등을 종합적으로 검토했습니다.
○ 주요 평가 내용은 비임상 유전독성, 피부감작성, 피부자극성, 급성독성, 반복투여독성, 생식발생독성, 피부흡수 등이며 결과는 다음과 같습니다.
1) 비임상 유전독성 시험* 자료를 검토한 결과 1,2,4-THB 성분을 세포 유전물질(DNA)에 변이를 일으키는 등 잠재적인 ‘유전독성’을 배제할 수 없는 물질로 평가했습니다.
* (유전독성시험) 세포의 DNA 및 염색체의 손상을 평가하는 비임상 시험으로 잠재적인 발암성 또는 돌연변이 유발물질을 검출할 목적으로 수행하며 OECD 가이드라인에는 박테리아를 이용한 복귀돌연변이시험 등 표준화된 방법이 제시되어 있음
2) 한편, 피부감작성, 피부자극성, 급성독성, 반복투여독성, 생식발생독성, 피부흡수 시험자료를 검토한 결과 1,2,4-THB 성분은 피부감작성 및 약한 피부자극성 물질로 평가되었습니다.
<전문가 자문회의 결과>
□ 전문가 자문 회의*에서는 1,2,4-THB의 유전독성 가능성을 배제하기 어렵다고 평가했으며, 유전독성 물질의 경우 사용량이나 사용환경 등과 무관하게 사용을 금지하는 것이 타당하다고 결론지었습니다.
* 독성·위해평가·화학 분야 전문가, 피부과 전문의 등으로 구성
□ 식약처는 앞으로 규제심사 등 후속 절차를 거쳐 올해 상반기 중 고시 개정 절차를 완료할 계획이며, 고시 개정일 이후 6개월 후부터는 해당 성분을 화장품 제조에 사용할 수 없도록 조치할 예정입니다.
○ 이번 결정은 비임상 시험결과 1,2,4-THB가 유전독성의 잠재적 가능성이 있고 피부감작성 물질로 평가되었지만,
- ▲생식·발생독성 등 다른 시험항목에서 중대한 위해성이 확인되지 않았고 ▲유럽이 사용금지 목록에 추가한 후 경과조치를 두고 제조·판매 금지를 시행하고 있는 점을 감안했습니다.
□ 식약처는 앞으로도 지속적으로 ‘화장품 원료’의 위해평가를 실시하고 외국의 규제현황을 모니터링 하는 등 규제과학을 바탕으로 국민에게 안전한 화장품을 공급할 수 있도록 최선을 다하겠습니다.
<붙임>
1. 식약처 위해평가 결과 요약
2. 안전기준 개정(안)에 대한 전문가 회의 결과
3. Q & A
▶붙임 1. 식약처 위해평가 결과 요약
(배경 및 경과) 유럽 SCCS에서 1,2,4-THB에 대한 위해평가 수행중이라는 정보가 입수되어 1,2,4-THB 위해평가 연구사업 수행(‘19.4-’20.11)
* (유럽 SCCS) 화장품 등 소비재에 사용되는 성분에 대한 안전성평가를 수행하는 유럽집행위원회 산하 독립적 과학자문기구이며, 안전성 검토 시 산업계 등으로 부터 자료를 제출받아 전반적인 문헌 고찰을 통해 평가
(검토자료) 1,2,4-THB에 대한 SCCS 위해평가 자료(피부흡수율, 피부자극성, 피부감작성, 유전독성, 급성독성, 반복투여독성, 생식발생독성 등) 및 관련 문헌
(대상물질) 1,2,4-THB 단독 (단, 피부흡수율 시험의 경우 1,2,4-THB‧PTD 복합물 사용) * PTD(p-toluenediamine) : 염모와 관련한 주요 물질
(결과)
- 유전독성시험 자료를 검토한 결과, 박테리아를 이용한 복귀돌연변이시험에서 명확한 양성의 결과가 나타났으며, 사람 유래 세포 등에서도 DNA 손상 및 염색체 이상을 유발하는 결과를 확인하였음
- 마우스를 이용한 피부감작성시험 결과, 상당한 피부감작성을 유발하였음
- 토끼를 이용한 피부자극성 시험 결과, 약한 피부자극성을 나타내었음
- 반복투여독성, 생식발생독성 등 다른 독성 시험에서는 중대한 위해성이 확인되지 않았음
(결론) 1,2,4-THB는 약한 피부 자극성 및 피부감작성 물질로 분류되며, 잠재적인 유전독성 가능성을 배제할 수 없음
▶붙임 2. 안전기준 개정(안)에 대한 전문가 회의 결과
□ 1차 회의(‘21.12.9)
(안건) 1,2,4-THB의 위해성에 대한 판단 및 안전기준 반영의 타당성, 유통 중 제품의 처리방향
(회의결과) 해당 물질에 대한 유럽 SCCS 보고서 등을 검토할 때 비임상실험 결과 유전독성 및 피부감작성의 우려가 제기되어 사전 예방적 안전관리 차원에서 사용을 금지하는 게 필요
- 다만, 인체에서의 직접적인 심각한 부작용 사례가 보고되지 않았고, 유럽에서도 충분한 경과조치(‘20.12월 고시, ’21.9 생산중지, ‘22.6월 판매중지)를 둔 점을 고려하여 시행시기 유연화 필요
□ 2차 회의(‘22.1.18)
(안건) 행정예고시 제출된 아래 주요의견에 대한 검토
- EU 금지는 염모제에 한한 것으로 제품내 1,2,4-THB 함유량, 사용시간, 함께 사용되는 물질의 조건을 고려하여 위해성을 제한적으로 평가해야 하며, 이 경우 샴푸는 조건에 해당하지 않음
- 안전성에 대한 추가 자료검토 및 과학적이고 공개적인 추가 실험 수행을 통한 위해성 검증 필요
(회의결과)
- 유전독성은 제품의 사용형태, 사용량 또는 빈도 등을 평가하여 안전역을 구하는 것이 의미가 없으며, 1,2,4-THB는 해당 물질 자체의 유전독성 우려로 인해 샴푸를 포함하여 금지 필요
- 안전성에 대한 업체의 현재 제출자료나 추가적 시험을 통한 완제품의 안전성 확보에도 기존 자료가 이미 충분하여 현행 유전 독성에 대한 판단이 달라지지 않음
▶붙임 3. Q & A
Q1. 1,2,4-THB는 어떤 성분인지
옅은 베이지색의 가루로 물에 잘 녹고 공기 중의 산소와 자발적으로 반응하여 검은색의 불용성 물질을 생성하며, 직접 모발염색 제품의 원료로 사용됩니다.(1,2,4-THB SCCS 보고서 2019, 9·13·14·15쪽 등)
유럽 SCCS 보고서(2019)에 따르면 화장품에서는 1,2,4-THB는 산화제 혼합 없이 영구염모제에는 최대 3%까지, 모발 염색샴푸(coloring shampoo)에서는 최대 0.7%까지 사용되고 있었습니다.
* (유럽의 조치경과) 1,2,4-THB 화장품 사용금지 목록 추가(’20.12∼) --> 화장품 생산에 사용금지(’21.9∼) --> 판매금지(’22.6∼)
Q2. 식약처의 1,2,4-THB 금지조치의 근거인 위해평가를 언제·어떻게 실시하였는지
1,2,4-THB는 2019년 유럽 SCCS에서 검토 중인 상황을 인지하고,
- 2019년 4월부터 관련 자료에 대한 조사 및 검토를 시작했으며, 2020년 11월 1,2,4-THB에 대한 위해평가를 최종 완료하였습니다.
화장품 중 해외 위해정보를 상시적으로 모니터링하여 안전관리에 반영하고 있습니다.
Q3. 유럽 SCCS의 위해성 지적은 1,2,4-THB를 단독으로 사용하는 경우에도 해당되는지
1,2,4-THB를 단독 사용한 유전독성 시험에서 유전독성 우려가 있다고 평가되었으므로 다른 염모성분의 사용 유무와 관계없이 1,2,4-THB가 들어가는 화장품은 유전독성 우려를 배제할 수 없습니다.(1,2,4-THB SCCS 보고서 2019, 15쪽)
Q4. 유럽 SCCS 평가보고서의 유전독성시험은 어떤 내용이었는지
사람 유래 세포 등을 이용한 유전독성 시험 결과를 종합적으로 검토한 결과 1,2,4-THB가 양성의 결과가 확인되었으므로, 인체 사용 시 유전독성의 우려를 배제할 수 없습니다.(1,2,4-THB SCCS 보고서 2019, 35-36쪽)
Q5. 1,2,4-THB 성분 관련 미국 등 외국현황은 어떠한지
국가별로 화장품 성분이나 제품을 관리하는 방식이 상이하며, 외국에서의 정확한 현황은 확인되지 않고 있습니다.
- 다만, 금번 식약처의 조치는 유럽의 평가보고서, 식품의약품안전평가원의 위해평가 결과, 외부 전문가 자문 등 근거에 기반하여 검토·평가하여 내린 결과입니다.
Q6. 화장품의 유형(예, 씻어내는 샴푸)에 따른 안전성은 어떠한지
전문가 회의 결과에 따르면 씻어내는 샴푸일지라도 ①모공이 있어 흡수율이 높은 두피에 ②직접 마사지하여, ③자주 사용하는 샴푸의 특징을 고려할 때 흡수율이 적다고 판단하기도 어렵다는 의견이 제시된 바 있습니다.
Q7. ‘염색이 되는 샴푸’를 유통판매하려면 어떤 절차를 거쳐야 하는지
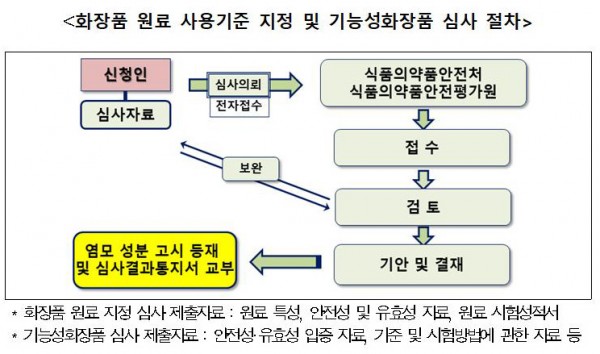
현재 ‘모발의 색상을 변화시키는 기능을 가진 화장품’(일시적인 경우는 제외)은 효능(염모력)을 입증하는 자료와 안전성 자료를 구비하여 기능성화장품으로 심사를 받고 유통판매가 가능하며,
- 만약 기존에 염모제 성분으로 고시에 등재되어 있지 않은 신규 염모 성분을 사용할 경우 심사와 동시에 등재절차를 진행하면 됩니다.
- 현재 해당 기능성화장품의 경우 유형에 제한이 없어 ‘염색이 되는 샴푸’도 심사 신청이 가능합니다.
Q8. 신기술 원료는 어떻게 사용할 수 있는지?
식약처는 새로운 기술을 활용한 제품이 안전 기준을 충족한 상태에서 신속하게 국민에게 제공될 수 있도록 제품화 상담과 지원을 적극적으로 하고 있으며, 이는 모든 개발자에게 열려 있습니다.
- 신기술 원료인 경우「화장품법」제8조제6항에 따라 현재까지 지정·고시되지 아니한 원료에 대한 사용기준을 지정·고시할 수 있도록 민원을 신청할 수 있습니다.
다만, 신기술의 지원이 해당 제품을 사용하는 국민의 안전보다 우선될 수는 없습니다. 국민이 안심할 만큼의 안전을 확보하기 위해서는 과학적 기준과 규정을 준수해야 하며, 이는 혁신적 기술이라고 해서 예외가 될 수 없습니다.
Q9. 대표적인 염모성분인 파라페닐렌디아민(PPD)는 심각한 감작성물질임에도 금지하지 않고 1,2,4-THB만 금지하는 이유는?
1,2,4-THB를 금지하는 주된 이유는 유전독성 및 피부감작성에 대한 잠재적 가능성이 있어서입니다.
파라-페닐렌디아민(PPD)의 경우 감작성 물질이긴 하나, 유전독성이나 발암성은 없는 것으로 평가되었습니다.(유럽 SCCS 위해평가, 2012.6.26)
* PPD(파라-페닐렌디아민) : 산화형염모제에 2.0% 제한(우리나라, 유럽, 일본)
식약처는 해외 안전기준 등을 상시적으로 모니터링을 하고 있으며, 식품·의약품과 관련한 안전성과 위해 가능성 등을 검토하여 국내 기준을 정비하고 있습니다.































댓글목록
등록된 댓글이 없습니다.